醫用高分子材料主要應用于生理系統疾病的診斷、治療、修復或生物體組織、器官的替換等,根據來源可以分為天然醫用高分子材料和合成醫用高分子材料2大類。
?
與天然高分子材料相比,合成醫用高分子材料往往具有更穩定的表面性質結構和多功能性,而且合成醫用高分子材料可以通過改變單體結構或相對分子質量來控制物理化學性質,這一特點使其研究方向從尋找合適的合成材料變為主動創造具有所需功能的新型材料,應用優勢更為明顯。
?
因此,合成高分子材料常用于制作植入物、人工臟器、人體導管等醫療器械。
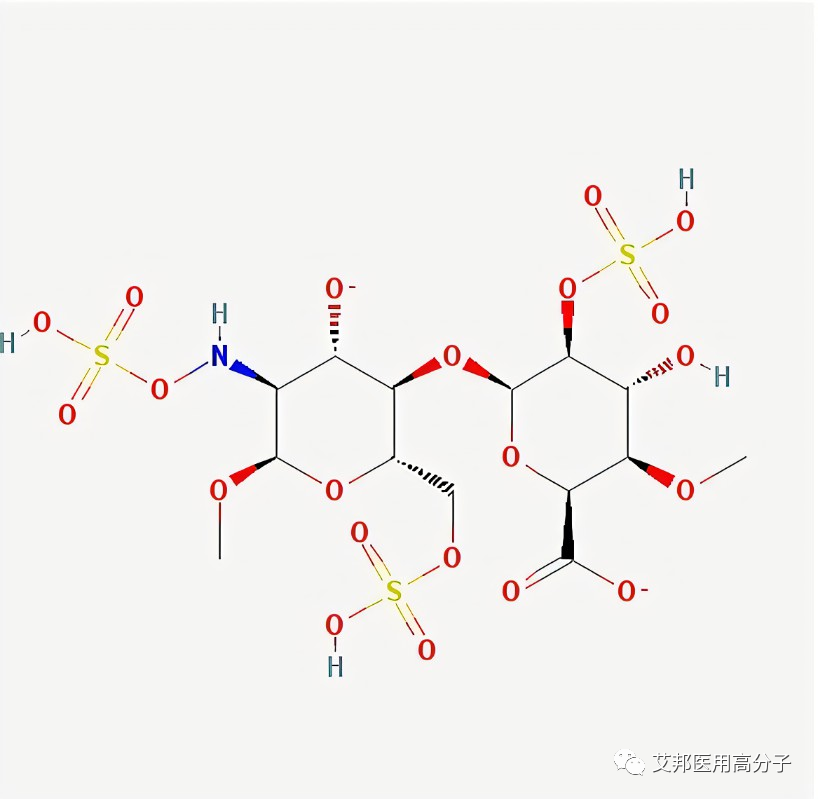
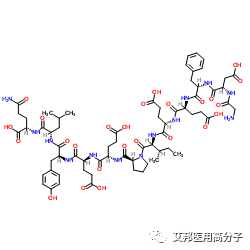
傳統的合成醫用高分子材料在接觸血液時,血液內的血漿蛋白會迅速吸附在表面,形成一層血漿蛋白層,該蛋白層會引發血小板的聚集和活化,進而導致局部凝血或血栓的產生。這一性質使得合成醫用高分子材料在生物醫學方向的發展受到了限制。因此,提高抗凝血性是合成醫用高分子材料的主要研究與發展方向之一。目前有關合成醫用高分子材料的抗凝血改性方向主要集中在控制非特異性血漿蛋白吸附和血小板黏附上,較為常見的方法就是對材料進行表面修飾,這是在不影響基體體積和特性的情況下將新的特性或功能整合到現有材料中的有效方法。肝素是一種黏多糖硫酸脂類抗凝血藥物,本身含有大量的負電荷,可以通過離子或共價鍵合的方式與合成醫用高分子材料結合以提高材料的抗凝血性質。近幾十年來,分子質量在3~30kDa的天然肝素是最常用于制造抗凝生物材料的表面修飾試劑之一,但有效性和生物活性很大程度上取決于固定化策略,因此,需要根據不同合成醫用高分子表面的物理化學性質選擇最有效的方法。目前合成醫用高分子材料常用的肝素化策略主要有共價鍵合、靜電沉積和共混。其中共混和靜電沉積均為物理摻入策略,對肝素活性位點的影響較小;共價鍵固定法在持久性和穩定性上更勝一籌。相應的,共混會使大多數肝素分子困在聚合物之中,導致肝素的利用率較低;靜電沉積策略缺乏耐久性,肝素易被血液中的陰離子物質取代,導致肝素爆發性釋放;共價鍵合在一定程度上會破壞肝素的結構和有效性。綜上,這幾種方法均有各自的優勢和缺陷,單獨作用時很難得到長期良好的抗凝效果。Li等通過兩步肝素摻入法,結合共價鍵合和靜電層層自組裝的方法制備了有效的長期抗凝聚己內酯(PCL)材料,這種方法的肝素吸附量(2.98μg/cm2)高于共價移植肝素法(0.63μg/cm2),體外釋放1個月后,PCL表面仍有1.10μg/cm2肝素殘留。岳秀麗等通過全氟磺酸靜電吸引重氮樹脂和肝素制備了靜電自組裝多層膜,然后光誘導重氮基團與硫酸鹽基團反應生成膜內層間共價鍵從而形成了穩定的肝素多層膜,在37℃的緩沖溶液中儲存10d后依舊保持良好的抗凝血活性。通過此類研究發現,結合靜電沉積和共價鍵合的策略既能改善肝素的穩定性,又能確保肝素在表面的活性和持久性。肝素常與其他物質共同作為有效成分來賦予合成醫用高分子材料多種功能。一氧化氮(NO)在抑制血小板黏附、激活和聚集中起到關鍵生理作用,肝素與NO的協同互補作用能夠快速實現抗凝血功能,同時促進材料表面內皮化,實現材料的長效抗凝血。Zhu等制備了一種聯合肝素和偶氮二醇鹽的心血管支架涂層,通過將肝素/偶氮二醇鹽共價移植到支架上,實現了肝素和NO的持續釋放。肝素除了與其他抗凝材料協同作用外,還常與抗菌性物質聯合作為功能涂層。Jin等將肝素和抗菌羧甲基殼聚糖結合到涂覆著聚多巴胺的聚氨酯膜表面,制備出具有良好血液相容性的植入材料。這一類的合成醫用高分子材料改性是將2個或多個具有協同和互補作用的功能性物質集成到材料表面,充分發揮了合成醫用高分子多功能性的優點,有助于材料獲得多種生物醫學應用功能。雖然肝素作為體內外都有抗凝血作用的物質應用范圍在不斷擴大,但在實際使用中存在多種并發癥,其中最主要的并發癥是自發性出血。大量使用肝素時可能會出現黏膜出血、傷口出血、內臟出血,還有可能會誘導產生血小板減少癥,嚴重時可引起胃腸道大量出血和中樞神經系統內出血,危及生命。因此,并發癥的威脅使得肝素的使用領域受到了極大限制。由于肝素來源于生物體,價格昂貴且可能會存在并發癥,模擬肝素的聚合物成為了一種有價值的抗凝劑替代策略,類肝素物質的研究和合成也成為近幾年的重要研究方向。Liu等通過自由基聚合首次合成了兩親性類肝素共聚物,并通過疏水-疏水相互作用固定在聚乳酸膜表面,在聚合物膜或透析器上構建了抗凝涂層。Nahain等使用可逆加成斷裂鏈轉移聚合法制備了一系列線性、水溶性的陰離子聚合物,并評估了這些聚合物的抗凝性能和它們作為肝素模擬物的用途,抗凝試驗表明,所有磺化均聚物和3種由磺化單體與丙烯酸組成的共聚物都是有效的抗凝劑。磺化殼聚糖是基于肝素的2個主要組成元素——含糖和磺酸鹽單元而開發的類似聚合物[。磺化殼聚糖及其衍生物與肝素的結構相似,通過對甲殼質和殼聚糖的磺化修飾以增加對血漿蛋白和血小板的靜電排斥從而減少血栓形成,可用于合成醫用高分子材料改性涂層。與肝素相比,磺化殼聚糖一方面增加了材料的表面親水性,另一方面增加了表面負電荷,使得蛋白質和材料表面之間產生更大的靜電斥力,因此這類物質更不易吸附蛋白質,血小板的黏附也更低。另外,殼聚糖可以從漁類制造工業產生的殘留物中獲得,這使得磺化殼聚糖及其衍生物比肝素成本低很多。天然水蛭素是從水蛭及其唾液腺中提取出的活性成分,是一種由65個氨基酸殘基組成的多肽,可以與凝血酶的催化中心發生不可逆的結合而使凝血酶失活,是迄今為止所發現最強的凝血酶天然特異性抑制劑。與肝素相比,水蛭素作為抗凝血藥物具有很多自身優勢,用藥量小,不引起出血,且具有蛋白質的兩親性,可以穩定吸附在合成醫用高分子材料的疏水表面。然而這種表面吸附可能會改變水蛭素的性質,并可能消除水蛭素抑制凝血酶的能力。另外,在血漿環境中,材料表面吸附的水蛭素可能被更高濃度或更強親和性的蛋白質所取代。因此,如果未來能夠找到方法使醫用合成醫用高分子材料吸附的水蛭素既保留抗凝血酶活性,又不會被血漿蛋白完全取代,那么水蛭素包覆的材料可能比肝素包覆的材料在成本和治療效果上更有優勢。檸檬酸是除肝素外另一個廣泛使用的抗凝劑,是一種弱有機酸,也是一種天然的防腐劑。檸檬酸鹽以檸檬酸鈉或檸檬酸葡萄糖的形式存在,在臨床治療中用于破壞凝血級聯反應來防止凝血。檸檬酸是一種小分子,常與其他聚合物結合來制備合成醫用高分子表面的功能性涂層。Yang等證明,通過檸檬酸和1,8-辛二醇縮聚合成的可生物降解彈性體具有優異的親水性和生物相容性,可以減少擴張聚四氟乙烯血管移植物上的血栓形成。除了上述的藥物之外,近年來還發現一些具有良好抗凝血效果的“候選抗凝劑”,如解聚海參糖胺聚糖(DHG)、甘草酸苷等。
這種抗凝劑不像華法林、阿加曲班、比伐盧定這類藥物只有在釋放到血液中時才有效,而是可以用于材料表面改性。但這些藥物用于合成醫用高分子材料表面涂層時的抗凝血效果以及制備工藝的難度還需要在之后的研究中進一步探索。提高表面親水性是將抗凝血性質引入合成醫用高分子材料的常見方法之一。親水性表面通常是通過將親水性物質接枝到材料表面獲得。抗凝機理是在合成醫用高分子表面創建一個水溶表層來減少血漿蛋白質、血小板的吸附,進而減少凝血和血栓的發生幾率。親水性改性的常見方法是在合成醫用高分子材料表面構建一層親水涂層。一些生物相容性強的親水材料常被作為改性合成醫用高分子的功能物質,如羥基磷灰石、聚環氧乙烷(PEO)、聚乙烯吡咯烷酮(PVP)等。近年來也有一些親水性物質被研究用于合成醫用高分子的抗凝涂層。Du等研究了一種由殼聚糖/聚乳酸-己內酯構成的心血管支架,并在支架上自組裝硫酸葡聚糖從而進行親水性改性,有效提高了支架的抗凝血性能。Zhu等利用CuSO4/H2O2引發聚多巴胺和聚甲基丙烯酸磺基甜菜堿共沉積工藝來賦予聚氨酯功能性涂層,該涂層可顯著提高材料表面的潤濕性,降低蛋白質吸附,從而改善血液相容性。這類親水涂層可以賦予合成醫用高分子材料良好的血液相容性,同時也可以與其他抗凝、抗菌材料或藥物聯合使用,為材料在血液中長期有效的應用提供參考思路。一些具有強親水性和電中性的生物堿可以與合成醫用高分子材料的表面結合,有效防止蛋白吸附、細胞黏附等不利的生物反應,例如2-甲基丙烯酰氧乙基磷酸膽堿(MPC)及其聚合物。這種聚合物具有良好的抗血栓形成性和生物相容性,即使在沒有抗凝劑的情況下,聚合物也會抑制蛋白質和細胞對接觸材料的吸附和黏附。因此,這些聚合物被廣泛用于修飾表面和提高醫療設備的整體生物相容性。Kalaska等合成了一種可以延長體內和體外凝血時間的共聚物,這種共聚物含有陰離子聚(2-丙烯酰胺-2-甲基丙磺酸鈉)作為抗凝成分,實驗證明擁有良好的抗凝功效和安全性。大多數抗凝血材料由含有硫酸鹽、磺酰胺、羧基和羥基的聚合物組成,研究認為這些離子官能團對抗凝活性具有有益的作用。由于—SO3H、—COOH和—OH等重要官能團的存在,所合成的聚合物材料可延緩血液凝固,尤其像硫酸根陰離子基團在血液中表現出與肝素類似的生物活性,可以絡合凝血因子,從而提高抗凝血能力。Alfieri等制備了硫酸化酚醛聚合物并研究它的抗凝原理,實驗發現這類化合物對內源性凝血途徑有良好的抑制作用。Ran等以端羧基三硫代碳酸酯為鏈轉移試劑,通過可逆加成-斷裂鏈轉移法聚合合成了一系列帶負電荷的大分子(NCMs),合成的NCMs具有延緩凝血的作用,可作為表面修飾添加劑,改善傳統合成醫用高分子材料的血液相容性。總之,近年來,國內外學者為合成醫用高分子材料表面的抗凝血性研究提供了許多新的思路,但現存的抗凝改性方法仍然具有或多或少的不足之處。如:(1)抗凝血功能的安全性、穩定性和有效性難以保證。(2)降低了合成醫用高分子材料自身優異的機械性能。(3)生產制備工藝過于復雜,成本造價過高,難以批量生產。種種制約條件使得合成醫用高分子材料的抗凝血改性是一條既難走,但又十分具有發展前景的研究道路。隨著科學技術的不斷發展,相信在不久的將來,這些限制因素會被逐步解決,讓合成醫用高分子材料為醫療行業發揮最大的作用。參考資料:馬慧君等,合成醫用高分子材料的抗凝血改性研究進展【J】現代化工,2022,12
原文始發于微信公眾號(艾邦醫用高分子):合成醫用高分子材料的抗凝血改性研究進展